O que é um Átomo?
Entenda a estrutura básica da matéria e os componentes fundamentais que formam tudo no universo.
O que é tudo isso?
Você já parou para pensar do que as coisas são feitas? Desde os objetos na sua casa até as árvores, o céu, a água e até mesmo você. Tudo que existe no universo é formado por partículas minúsculas chamadas átomos. Eles são tão pequenos que ninguém consegue vê-los a olho nu, nem mesmo com uma lupa. Para observá-los, os cientistas precisam usar instrumentos superpotentes chamados microscópios eletrônicos.
Os átomos são a base de toda a matéria. Isso significa que tudo o que tem massa e ocupa espaço é feito de átomos. Um único grão de areia contém trilhões e trilhões deles! E o mais incrível: embora existam muitos tipos diferentes de coisas no mundo, tudo é feito de combinações dos mesmos átomos.
Durante muito tempo, as pessoas acreditavam que a matéria podia ser dividida infinitamente. Só que, há mais de dois mil anos, um filósofo chamado Demócrito teve uma ideia diferente. Ele disse que existia um ponto onde não dava mais para dividir: esse ponto invisível e indivisível ele chamou de “átomo”, que em grego quer dizer “indivisível”. Claro, ele não tinha como provar isso naquela época, mas hoje sabemos que ele estava certo em muitas partes.
Aprender sobre átomos é entender como o universo é construído. É como descobrir os tijolinhos invisíveis de tudo o que existe! Nos próximos capítulos, vamos explorar melhor o que são os átomos, como eles funcionam e por que eles são tão importantes para a nossa existência.
O átomo: o tijolinho de tudo
Imagine que o universo é uma construção gigantesca. Para levantar qualquer estrutura, você precisa de blocos ou tijolos, certo? Pois bem, os átomos são esses tijolos fundamentais da natureza. Eles são as menores partes da matéria que ainda conservam as propriedades de um elemento. Pense neles como as peças de LEGO que se encaixam para formar tudo o que existe — desde uma flor até uma estrela!
Mesmo que você não os veja, os átomos estão aí: no ar que entra no seu pulmão, na água que você bebe, na tela do seu celular e em cada célula do seu corpo. E o mais impressionante: apesar de minúsculos, eles formam estruturas imensas. Um simples copo de água, por exemplo, contém cerca de 1024 moléculas, e cada molécula é feita de átomos!
Existem mais de 100 tipos diferentes de átomos, e cada tipo é chamado de elemento químico. Alguns exemplos são o hidrogênio, o oxigênio, o carbono, o ferro e o ouro. Esses elementos estão organizados na Tabela Periódica, uma ferramenta que os cientistas usam para estudar e entender melhor a matéria.
Quando dois ou mais átomos se ligam, eles formam moléculas. Por exemplo, a água é formada por dois átomos de hidrogênio e um de oxigênio – H2O. Já o sal de cozinha é uma combinação de sódio e cloro – NaCl. A variedade das coisas que existem no mundo se deve às diferentes formas com que os átomos podem se juntar.
Tudo começa com o átomo. Mesmo sendo invisível, ele é o tijolinho essencial de tudo o que conhecemos. E quanto mais você entende sobre ele, mais você entende sobre o funcionamento do universo.
Como é um átomo por dentro?
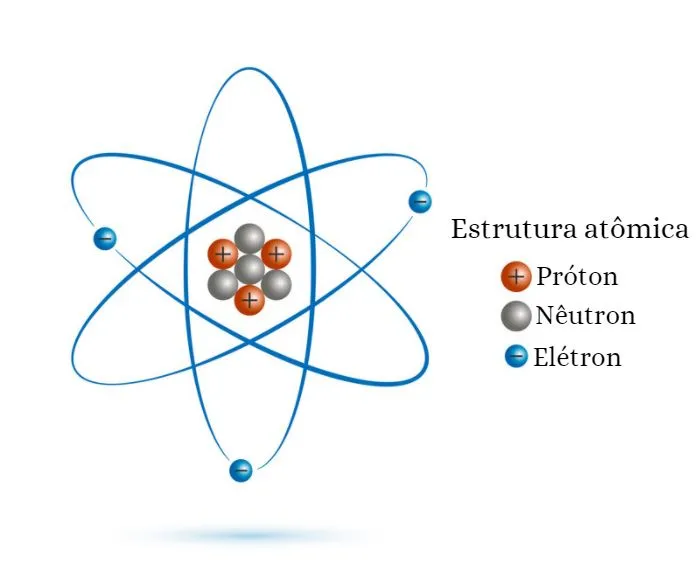
Agora que você já sabe que tudo é feito de átomos, está na hora de descobrir como eles são por dentro. Você pode imaginar um átomo como um pequeno sistema solar em miniatura. No centro dele, está o núcleo, uma parte extremamente densa e carregada de energia. Dentro do núcleo vivem duas partículas: os prótons (com carga positiva) e os nêutrons (sem carga).
Ao redor do núcleo, girando em regiões chamadas de camadas eletrônicas ou níveis de energia, ficam os elétrons. Essas partículas são bem menores que os prótons e nêutrons e possuem carga negativa. Os elétrons não seguem uma trajetória fixa, mas se movimentam muito rápido ao redor do núcleo, criando uma espécie de “nuvem eletrônica”.
Cada átomo tem uma quantidade diferente de prótons, nêutrons e elétrons. Por exemplo, o átomo de hidrogênio tem apenas um próton e um elétron, sem nêutrons. Já o átomo de carbono tem seis prótons, seis nêutrons e seis elétrons. A quantidade de prótons no núcleo é o que define qual é o elemento químico daquele átomo.
Mesmo sendo tão pequenos, os átomos têm uma estrutura organizada e complexa. Entender como essa estrutura funciona ajuda os cientistas a prever como os elementos vão se comportar em diferentes situações. E isso é essencial para a química, a física, a biologia, e até para a tecnologia!
De que os átomos são feitos?
Você já sabe que o átomo tem um núcleo no centro e elétrons ao redor. Mas vamos olhar mais de perto: de que são feitas essas partes? Um átomo é composto por três partículas subatômicas principais:
1. Prótons: Estão no núcleo e têm carga positiva (+). A quantidade de prótons define o tipo de elemento. Por exemplo, o átomo de oxigênio tem 8 prótons. Se mudar esse número, já não é mais oxigênio.
2. Nêutrons: Também ficam no núcleo, mas não têm carga — são neutros. Eles ajudam a manter o núcleo estável. Em alguns elementos, o número de nêutrons pode variar, dando origem aos isótopos.
3. Elétrons: Ficam fora do núcleo, girando ao seu redor. São muito leves e têm carga negativa (–). Os elétrons são responsáveis pelas ligações químicas entre os átomos, ou seja, por unir um átomo ao outro.
Essas três partículas formam a base de tudo o que existe. Mas a ciência moderna foi além e descobriu que até mesmo os prótons e nêutrons são formados por partículas ainda menores chamadas quarks. E os elétrons fazem parte de outra família de partículas chamadas léptons.
Esses estudos fazem parte da física de partículas, uma área que busca entender os menores pedaços do universo. É como se os átomos fossem peças de um quebra-cabeça, e os cientistas estivessem tentando descobrir como cada peça se encaixa.
Como os átomos se ligam e formam moléculas
Agora que você já sabe como os átomos são por dentro, vamos entender como eles se ligam entre si. Sozinhos, os átomos são interessantes, mas quando eles se unem, formam algo novo: as moléculas. É assim que surgem substâncias como a água, o açúcar, o oxigênio que respiramos e até os materiais de que são feitas as roupas e os plásticos.
Os átomos se ligam por meio de suas partículas externas: os elétrons. Eles podem compartilhar, doar ou receber elétrons de outros átomos, formando diferentes tipos de ligações químicas. A mais comum é a ligação covalente, onde dois átomos compartilham elétrons para se manter unidos. Também existe a ligação iônica, em que um átomo doa elétrons e o outro recebe.
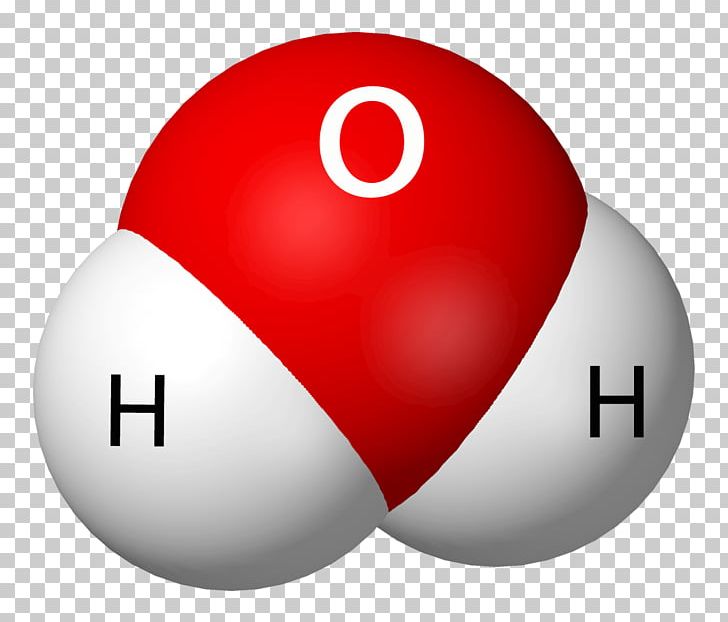
Por exemplo, a molécula de água (H2O) é formada por dois átomos de hidrogênio e um de oxigênio. Os elétrons desses átomos são compartilhados, criando uma ligação covalente. Outro exemplo é o sal de cozinha (NaCl), formado por átomos de sódio e cloro que se ligam por uma ligação iônica.
Cada tipo de molécula tem propriedades diferentes. Algumas são sólidas, outras líquidas ou gasosas. Algumas conduzem eletricidade, outras não. Tudo isso depende de como os átomos estão organizados e de que tipo de ligações eles fazem.
Portanto, é a maneira como os átomos se ligam que permite a diversidade de tudo que conhecemos. Se os átomos fossem apenas partículas soltas, o universo seria um lugar bem monótono. Mas como eles se combinam de muitas formas, surgem cores, cheiros, sabores, sons, objetos... e até a vida!
Compreender o átomo é fundamental para avançar no estudo das ciências naturais e entender o funcionamento do universo em sua escala mais básica.
O que é tudo isso?
Você já parou para pensar do que as coisas são feitas? Desde os objetos na sua casa até as árvores, o céu, a água e até mesmo você. Tudo que existe no universo é formado por partículas minúsculas chamadas átomos. Eles são tão pequenos que ninguém consegue vê-los a olho nu, nem mesmo com uma lupa. Para observá-los, os cientistas precisam usar instrumentos superpotentes chamados microscópios eletrônicos.
Os átomos são a base de toda a matéria. Isso significa que tudo o que tem massa e ocupa espaço é feito de átomos. Um único grão de areia contém trilhões e trilhões deles! E o mais incrível: embora existam muitos tipos diferentes de coisas no mundo, tudo é feito de combinações dos mesmos átomos.
Durante muito tempo, as pessoas acreditavam que a matéria podia ser dividida infinitamente. Só que, há mais de dois mil anos, um filósofo chamado Demócrito teve uma ideia diferente. Ele disse que existia um ponto onde não dava mais para dividir: esse ponto invisível e indivisível ele chamou de “átomo”, que em grego quer dizer “indivisível”. Claro, ele não tinha como provar isso naquela época, mas hoje sabemos que ele estava certo em muitas partes.
Aprender sobre átomos é entender como o universo é construído. É como descobrir os tijolinhos invisíveis de tudo o que existe! Nos próximos capítulos, vamos explorar melhor o que são os átomos, como eles funcionam e por que eles são tão importantes para a nossa existência.
O átomo: o tijolinho de tudo
Imagine que o universo é uma construção gigantesca. Para levantar qualquer estrutura, você precisa de blocos ou tijolos, certo? Pois bem, os átomos são esses tijolos fundamentais da natureza. Eles são as menores partes da matéria que ainda conservam as propriedades de um elemento. Pense neles como as peças de LEGO que se encaixam para formar tudo o que existe — desde uma flor até uma estrela!
Mesmo que você não os veja, os átomos estão aí: no ar que entra no seu pulmão, na água que você bebe, na tela do seu celular e em cada célula do seu corpo. E o mais impressionante: apesar de minúsculos, eles formam estruturas imensas. Um simples copo de água, por exemplo, contém cerca de 1024 moléculas, e cada molécula é feita de átomos!
Existem mais de 100 tipos diferentes de átomos, e cada tipo é chamado de elemento químico. Alguns exemplos são o hidrogênio, o oxigênio, o carbono, o ferro e o ouro. Esses elementos estão organizados na Tabela Periódica, uma ferramenta que os cientistas usam para estudar e entender melhor a matéria.
Quando dois ou mais átomos se ligam, eles formam moléculas. Por exemplo, a água é formada por dois átomos de hidrogênio e um de oxigênio – H2O. Já o sal de cozinha é uma combinação de sódio e cloro – NaCl. A variedade das coisas que existem no mundo se deve às diferentes formas com que os átomos podem se juntar.
Tudo começa com o átomo. Mesmo sendo invisível, ele é o tijolinho essencial de tudo o que conhecemos. E quanto mais você entende sobre ele, mais você entende sobre o funcionamento do universo.

Como é um átomo por dentro?
Agora que você já sabe que tudo é feito de átomos, está na hora de descobrir como eles são por dentro. Você pode imaginar um átomo como um pequeno sistema solar em miniatura. No centro dele, está o núcleo, uma parte extremamente densa e carregada de energia. Dentro do núcleo vivem duas partículas: os prótons (com carga positiva) e os nêutrons (sem carga).
Ao redor do núcleo, girando em regiões chamadas de camadas eletrônicas ou níveis de energia, ficam os elétrons. Essas partículas são bem menores que os prótons e nêutrons e possuem carga negativa. Os elétrons não seguem uma trajetória fixa, mas se movimentam muito rápido ao redor do núcleo, criando uma espécie de “nuvem eletrônica”.
Cada átomo tem uma quantidade diferente de prótons, nêutrons e elétrons. Por exemplo, o átomo de hidrogênio tem apenas um próton e um elétron, sem nêutrons. Já o átomo de carbono tem seis prótons, seis nêutrons e seis elétrons. A quantidade de prótons no núcleo é o que define qual é o elemento químico daquele átomo.
Mesmo sendo tão pequenos, os átomos têm uma estrutura organizada e complexa. Entender como essa estrutura funciona ajuda os cientistas a prever como os elementos vão se comportar em diferentes situações. E isso é essencial para a química, a física, a biologia, e até para a tecnologia!
De que os átomos são feitos?
Você já sabe que o átomo tem um núcleo no centro e elétrons ao redor. Mas vamos olhar mais de perto: de que são feitas essas partes? Um átomo é composto por três partículas subatômicas principais:
1. Prótons: Estão no núcleo e têm carga positiva (+). A quantidade de prótons define o tipo de elemento. Por exemplo, o átomo de oxigênio tem 8 prótons. Se mudar esse número, já não é mais oxigênio.
2. Nêutrons: Também ficam no núcleo, mas não têm carga — são neutros. Eles ajudam a manter o núcleo estável. Em alguns elementos, o número de nêutrons pode variar, dando origem aos isótopos.
3. Elétrons: Ficam fora do núcleo, girando ao seu redor. São muito leves e têm carga negativa (–). Os elétrons são responsáveis pelas ligações químicas entre os átomos, ou seja, por unir um átomo ao outro.
Essas três partículas formam a base de tudo o que existe. Mas a ciência moderna foi além e descobriu que até mesmo os prótons e nêutrons são formados por partículas ainda menores chamadas quarks. E os elétrons fazem parte de outra família de partículas chamadas léptons.
Esses estudos fazem parte da física de partículas, uma área que busca entender os menores pedaços do universo. É como se os átomos fossem peças de um quebra-cabeça, e os cientistas estivessem tentando descobrir como cada peça se encaixa.
Como os átomos se ligam e formam moléculas
Agora que você já sabe como os átomos são por dentro, vamos entender como eles se ligam entre si. Sozinhos, os átomos são interessantes, mas quando eles se unem, formam algo novo: as moléculas. É assim que surgem substâncias como a água, o açúcar, o oxigênio que respiramos e até os materiais de que são feitas as roupas e os plásticos.
Os átomos se ligam por meio de suas partículas externas: os elétrons. Eles podem compartilhar, doar ou receber elétrons de outros átomos, formando diferentes tipos de ligações químicas. A mais comum é a ligação covalente, onde dois átomos compartilham elétrons para se manter unidos. Também existe a ligação iônica, em que um átomo doa elétrons e o outro recebe.
Por exemplo, a molécula de água (H2O) é formada por dois átomos de hidrogênio e um de oxigênio. Os elétrons desses átomos são compartilhados, criando uma ligação covalente. Outro exemplo é o sal de cozinha (NaCl), formado por átomos de sódio e cloro que se ligam por uma ligação iônica.
Cada tipo de molécula tem propriedades diferentes. Algumas são sólidas, outras líquidas ou gasosas. Algumas conduzem eletricidade, outras não. Tudo isso depende de como os átomos estão organizados e de que tipo de ligações eles fazem.
Portanto, é a maneira como os átomos se ligam que permite a diversidade de tudo que conhecemos. Se os átomos fossem apenas partículas soltas, o universo seria um lugar bem monótono. Mas como eles se combinam de muitas formas, surgem cores, cheiros, sabores, sons, objetos... e até a vida!

Compreender o átomo é fundamental para avançar no estudo das ciências naturais e entender o funcionamento do universo em sua escala mais básica.